全球艾滋病毒每年新感染180万人,这使研制艾滋病毒疫苗成为一项全球卫生高度重视的事项。几乎所有获得许可的疫苗都是通过诱导抗体进行保护的,但HIV和流感病毒等高度变异的病原体不受这种传统疫苗限制。近日,刊登在《Science》的两篇文章报告了关于HIV疫苗研究新进展。
在罕见的HIV阳性个体中发现了抗HIV的广泛中和抗体(bnAbs),这表明设计出有效的疫苗是可能的。然而,HIV疫苗的开发已经被证明是非常具有挑战性的,因为HIV靶向的bnAbs有许多不寻常的特征,包括位于正常突变基因点之外的“不可能的突变”。此外,已知bnAbs的前体推断通常对病毒没有可检测的亲和力。因此,疫苗接种需要首先对编码bnAb前体的B细胞进行预处理,然后用免疫原诱导抗体亲和力成熟,以获得不寻常的特征。
来自美国加利福尼亚州的Steichen等人。选择关注bnAbBG18,它通过重链互补决定区3(HCDR3)与HIV包膜蛋白上的保守位点结合,包含不可能突变的位点。它没有插入或删除基因片段,因此可能比其他bnAbs更容易诱导。
根据BG18与三聚体结合的晶体结构,以及低温电子显微镜和突变研究的结构和功能信息,研究者们能确定BG18识别靶的关键遗传特征。这些发现为从14个HIV阴性捐赠者的B细胞受体(BCR)重链序列中寻找潜在的BG18前体提供了生物信息学方法。研究发现在所有供体中都发现了前体,并利用其HCDR3结构域的序列信息设计了BG18前体抗体。
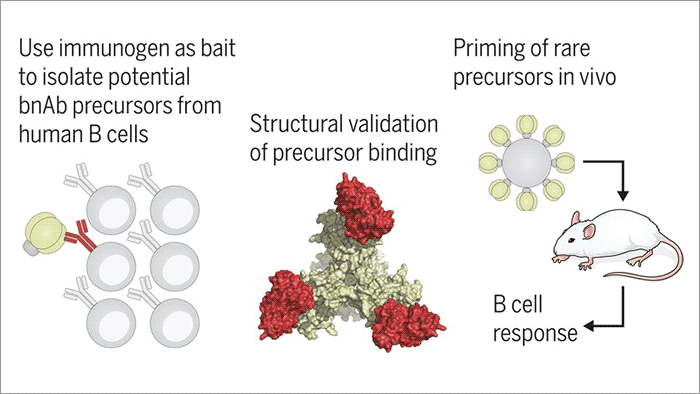
接下来,这些抗体被用作选择试剂,用于利用哺乳动物细胞表面显示库定向进化和优化三聚体免疫原。其中一种免疫原N332-GT2三聚体通过低温电子显微镜进行结构分析,它被发现以类似于天然三聚体与BG18结合的方式结合其选择抗体。
为了测试这种免疫原是否真的能启动BG18前体,研究者用非常低频率的BG18前体表达B细胞的小鼠。结果表明,含N332-GT2三聚体的免疫能诱导持续的生发中心反应和亲和力成熟。重要的是,他们还证明了免疫原可以与人类供体来源的罕见的原始B细胞结合,这些细胞编码类似BG18的前体。
而来自美国北卡罗来纳州杜克大学医学院的Saunders等人,提出假设有对bnAb前体具有中等到高等亲和力的免疫原、对有不可能突变形式更高亲和力的免疫原既可以启动bnAb前体B细胞,又可以诱导它们向bnAb发展。研究者们关注了bnAbs DH270和CH235,通过计算推断它们的克隆史来确定各自的未突变共同原型。结构模型使他们能合理地设计与未突变共同原型结合的免疫原,但结合其亲和力成熟的形式更加强烈。报告称用纳米免疫原接种疫苗确实是为突变不太可能的bnAbs选择的。诱导抗体的低温电子显微镜结构分析显示它们与部分成熟的bnAb前体相似。
设计用来诱导类CH235抗体的抗原在四只纯种恒河猴身上进行了检测。两个月一次的纳米抗原免疫过程在所有动物身上都产生了有效的中和抗体,这些抗体在其bnAb发育早期与CH235样抗体具有相似的中和特征。
这两项最新的研究表明,设计与bnAb前体结合的免疫原或选择特定的不可能突变的方法是可行的。这种方法也可用于设计针对其他病原体的疫苗的种系靶向免疫原。


